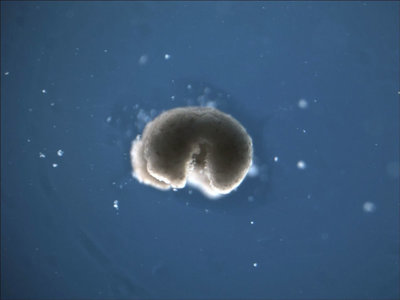
Из тканей лёгких человека вырастили существа, которые ползают и лечат окружающие клетки
Жизнь и смерть традиционно рассматриваются как противоположности. Но возникновение новых многоклеточных форм жизни из клеток мёртвого организма вводит "третье состояние", которое лежит за пределами традиционных границ жизни и смерти.
Смерть считается необратимой остановкой функционирования организма в целом. Однако такие практики, как пересадка органов, указывают на способность органов, тканей и клеток продолжать функционировать даже после гибели организма. Эта устойчивость поднимает вопрос о механизмах, которые дают такую возможность.
Вплотную изучением жизни после смерти занялись Питер А. Нобл с кафедры микробиологии Вашингтонского университета и Алекс Пожитков из Высшей школы биологических наук Ирелла и Манеллы в Национальном медицинском центре "Город надежды" в Калифорнии. Результатами своих изысканий они поделились в четверг на страницах The Conversation.
Третье состояние бросает вызов традиционным представлениям о поведении клеток. К нему не относятся гусеницы, превращающиеся в бабочек, или головастики, эволюционирующие в лягушек, а также опухоли, органоиды и клеточные линии, которые могут бесконечно делиться в чашке Петри, потому что они не развивают новые функции.
Зато клетки кожи, извлеченные из эмбрионов умерших лягушек, смогли адаптироваться к новым условиям в лаборатории, спонтанно реорганизовавшись в многоклеточные организмы, называемые ксеноботами. Эти организмы демонстрировали поведение, которое выходит далеко за рамки их первоначальных биологических ролей. В частности, ксеноботы используют свои реснички — небольшие, похожие на волоски структуры — для навигации и передвижения по окружающей среде, тогда как у живого эмбриона лягушки реснички обычно используются для перемещения слизи.
Кроме того, они способны осуществлять кинематическую саморепликацию, то есть могут физически воспроизводить свою структуру и функцию без роста. Это отличается от более распространённых процессов репликации, которые включают рост внутри или снаружи организма.
Отдельные клетки лёгких человека также могут самоорганизовываться в миниатюрные многоклеточные организмы, способные к передвижению. Эти антропоботы ведут себя и структурированы по-новому. Они не только могут ориентироваться в своем окружении, но и восстанавливать как себя, так и повреждённые нервные клетки, размещённые поблизости.
В совокупности эти результаты демонстрируют присущую клеточным системам пластичность и бросают вызов идее о том, что клетки и организмы могут развиваться только предопределёнными способами. Третье состояние предполагает, что смерть организма может играть значительную роль в том, как жизнь трансформируется с течением времени.
На способность к такому выживанию влияют разные факторы — такие, как условия окружающей среды, метаболическая активность и методы консервации.
Разные типы клеток имеют разное время выживания. Например, лейкоциты человека гибнут через 60-86 часов после смерти организма. У мышей клетки скелетных мышц можно вырастить заново через 14 дней после смерти, тогда как клетки фибробластов овец и коз можно культивировать до месяца после смерти.
Сложнее культивировать активные клетки, которым нужно много энергии для поддержания их функций. Продлевает выживаемость криоконсервация.
Врождённые механизмы выживания также играют существенную роль в судьбе клеток и тканей. Отмечено значительное увеличение активности генов, связанных со стрессом и иммунитетом, после смерти организма, что, вероятно, компенсирует потерю гомеостаза. Более того, такие факторы, как травма, инфекции и время, прошедшее с момента смерти, сильно влияют на жизнеспособность тканей и клеток.
Свойства некоторых тканей зависят даже от возраста, здоровья и пола того, у кого они взяты. Это хорошо заметно по приживаемости вырабатывающих инсулин островковых клеток поджелудочной железы при её пересадке.
Как взаимодействие всех этих переменных позволяет определённым клеткам продолжать функционировать после смерти организма, пока остаётся неясным. Как и потенциал перешедших в третье состояние клеток к трансформации.
Если всё это удастся выяснить, открываются поистине фантастические перспективы. Искусственно выращенные антропоботы могут стать доставщиками лекарств без запуска нежелательного иммунного ответа, растворять атеросклеротические бляшки, удалять избыток слизи у пациентов с муковисцидозом. А понимание механизма выключения (срок жизни любых многоклеточных антропоботов ограничен четырьмя-шестью неделями) научит наконец человечество лечить онкологию.
Фото: cdorgs.github.io/Kriegman, S., Blackiston, D., Levin, M., Bongard, J. (Creative Commons Attribution 4.0 International license)
Подписывайтесь на NewsInfo.Ru














